

利用 神经递质谷氨酸修饰的 Glu- UCNP 介导的 非侵入性 近红外 光遗传学调控 技术 促进 脊髓损伤后 脑-脊髓 神经 环 路 结构与功能重建
脊髓损伤( Spinal Cord Injury, SCI )是 一种严重的 中枢神经系统创伤性损伤 , 尽管在脊髓损伤的治疗方面已 取得了 诸多进展,但目前仍未找到能够完全治愈脊髓损伤的临床药物或 技术 。脊髓损伤的完全恢复需要精确重建复杂的神经环路,尤其是在恢复长 距离 投九游娱乐官方平台射轴突与靶向突触后神经元之间的连接方面,目前仍面临巨大挑战。 大脑 运动皮层中的皮质脊髓 束 神经元 发出 下行 皮质脊髓束( Corticospinal tract, CST ) 神经 轴突投射到脊髓,靶向连接脊髓中的突触后中间神经元, 将大脑皮层的运动指令传递至脊髓,调节脊髓中间神经元的活动,并进一步激活脊髓运动环路,发挥关键的 随意运动 ( voluntary movement ) 控制 作用。 CST 轴突的损伤会导致 脑 - 脊髓 投射 的 运动控制 功能丧失,而精确重建 CST 轴突与 脊髓 靶神经元之间的连接,对恢复运动功能至关重要。然而,如何 针对特定类型突触 精确地 重建 CST 轴突与靶神经元 之间 功能性神经连接,仍是脊髓损伤治疗中的核心问题。
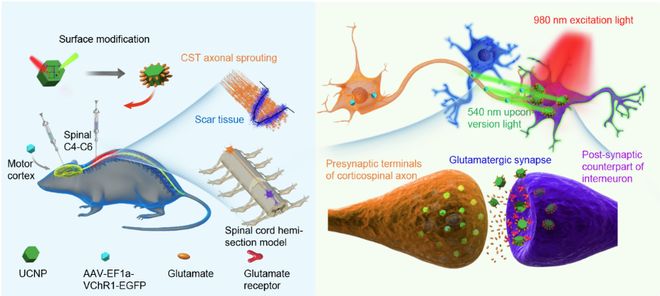
图 1 Glu-UCNP 介 导的 NIR 光遗 传学调控技术促进脊髓损伤后 CST 轴突与谷氨酸能 突触后 中间神经元重 新 连接 的 示意图 。
光遗传学 技术 能够在单细胞甚至亚细胞层面实现精准的神经 环路 调控,为神经环路的精确 重建 提供了前所未有的可能性。结合传统电生理方法,光遗传学工具已广泛应用于揭示长距离投射神经元的 作用靶点及其环路 机制, 同时 在运动调控方面展现出巨大的潜力。然而,传统体内光遗传学应用 通常 需要将光纤植入脑 或脊髓 组织,尽管能够实现深度刺激,但这种侵入性手术可能对动物带来 其它 风险,影响其行为 表现 ,并限制了 该技术的 应用范围。
为解决这一问题, 研究团队 提出了基于上转换纳米颗粒( Upconversion nanoparticles , UCNP )的非侵入性光遗传学调控策略。 UCNP 能将近红外( Near-infrared , NIR )光转换为可见光, 利用近红外光对组织的较强穿透能力, 从而在无需侵入性手术的情况下实现深部组织的远程光遗传学刺激。更重要的是, UCNP 表面可通过 特定神经递质 进行修饰,精准靶向特定类型 的神经元 ,从而实现 近红外 光遗传学 工具 对特定神经元类型的靶向 调控。
在本研究中, 研究 团队 构建了 谷氨酸( Glutamate , Glu ) 修饰 的 UCNP ( Glu-UCNP ) ,实现了对 SCI 后 CST 轴突再生和 神经环路 功能恢复的精准调控。 该系统利用了 CST 神经元是谷氨酸能神经元的特性, CST 投射到脊髓后主要与中间神经元连接,因此这些受 CST 支配的脊髓神经元主要为谷氨酸能突触的突触后中间神经元(即表达谷氨酸受体的脊髓中间神经元)。 该系统通过在 CST 神经元 中 表达 光敏感通道蛋白( Channelrhodopsin 1, ChR1 ),与 脊髓中 特异性摄取 Glu- UCNP 的 谷氨酸能 突触后中间神经元 相 配合,从而实现 CST 与靶 神经元之间的精准连接重建(图1)。
在此过程中, Glu-UCNP 扮演 了双重 功能 : 一方面, 移植到 SCI 后 脊髓 特定 区域 的 Glu-UCNP 能够 靶向 脊髓中 谷氨酸能突触的突触后神经元( 通过 与表达谷氨酸受体的脊髓中间神经元结合并被内化), 另一方面, 当 NIR 光照射脊髓 特定 区域时, 它充当 内部光转换器,将 NIR 光 转化为可激活 CST 中 ChR1 的可见光 。这一 光 转换过程 激活 了 表达 ChR1 的 受损 或残留 CST 轴突 再生 , 并引导 其朝向 脊髓中谷氨酸能突触的突触后中间神经元 (包括 V2a 中间神经元)重连 , 从而 重塑 了脑 - 脊髓 中枢运动 环路(图1)。
本 研究 通过活细胞成像、 脑 - 脊髓神经环路病毒示踪、 脊髓组织免疫荧光染色 等 实验 手段 , 观察到 Glu-UCNP 介导的 NIR 光遗传 学调控技术 不仅促进 了 损伤 CST 轴突的再生 ,还 引导其与谷氨酸能突触后中间神经元(包括 V2a 神经元)精确连接(图2)。 通过 体内钙离子 检测 和前肢精细运动 取食实验 验证了该 策略 对于功能重建的 有效 性(图3)。 这些结果进一步表明, Glu-UCNP 介导的 NIR 光遗传学调控技术促进 了 SCI 后脑 - 脊髓神经连接 的 结构和功能 重塑,进而有助于改善脊髓损伤引起的运动功能障碍。研究人员进一步通过对 激活 CST 神经元的单细胞 转录组测序 , 揭示了 Glu-UCNP 介导的 NIR 光遗传 学 调节过程中, CST 轴突再生相关分子网络的动态变化。这些发现不仅验证了该方法重建脑-脊髓精确连接的可行性,也为中枢神经系统损伤的临床治疗手段提供了有价值的研究基础。
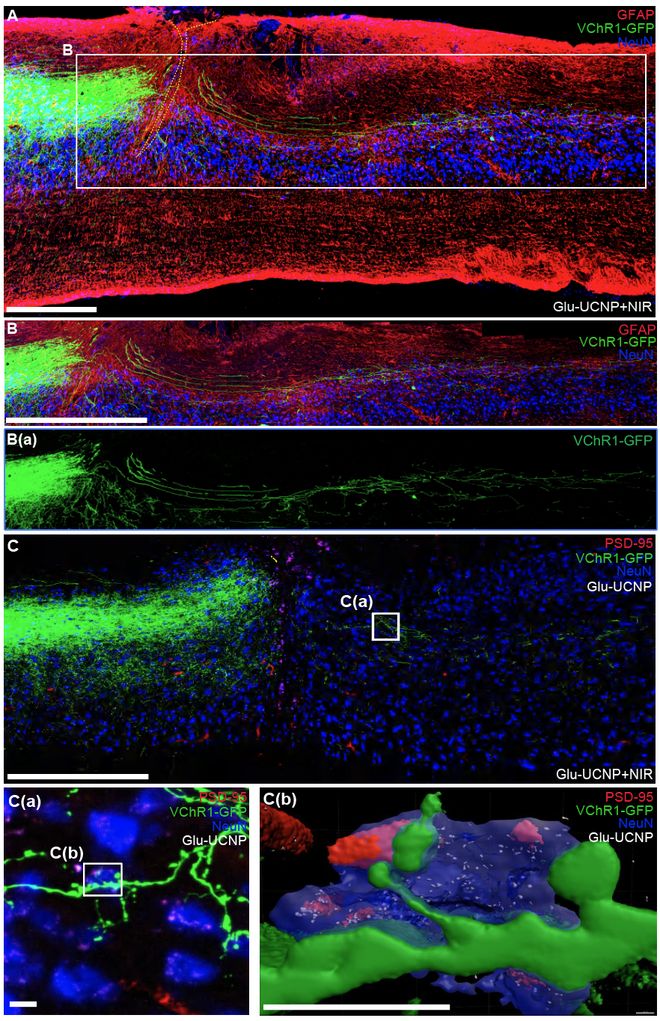
图 2 Glu-UCNP 介 导的 NIR 光遗传学 调控 技术 促进 脊髓损伤后 CST 轴突 芽生 并 与 脊髓 谷氨酸能突触后中间神经元 形成突触连接 。
苏州大学神经科学研究所刘耀波教授 为该文章的最后通讯作者, 苏州大学 功能纳米与 软 物质 学院的刘坚教授为文章的共同通讯作者,苏州大学神经科学研究所的博士研究生吉 喆 为本文的第一作者,苏州大学功能纳米与 软 物质 学院的博士后严俊为本文的共同第一作者。
刘耀波教授团队长期从事 脑 - 脊髓 中枢神经环路构建以及损伤修复的研究工作,致力于中枢神经再生的分子细胞调控机制和干预靶点、以及神经信号调控中枢神经环路重建的机制和关键技术的转化神经科学研究。在
 热点新闻
热点新闻  联系我们
联系我们 电话:13929967909
座机:0757-83205002
邮箱:19407036@qq.com
地址:广东省佛山市禅城区国际交易中心8座2楼30-31号

