

在多蛋白互作和相分离研究中,当前仍缺乏一种可同时实现实时成像、动态调控与功能分析的一体化通用平台。
为解决当前研究中在活细胞中同时监测多蛋白互作与相分离行为的技术难题,作者团队研究并开发了一种模块化、多功能的活细胞可视化工具:分子招募共定位系统(Molecular Recruitment Colocalization,MRC),可实现多蛋白互作与生物大分子凝聚体的同步可视化。 该研究成果近日以

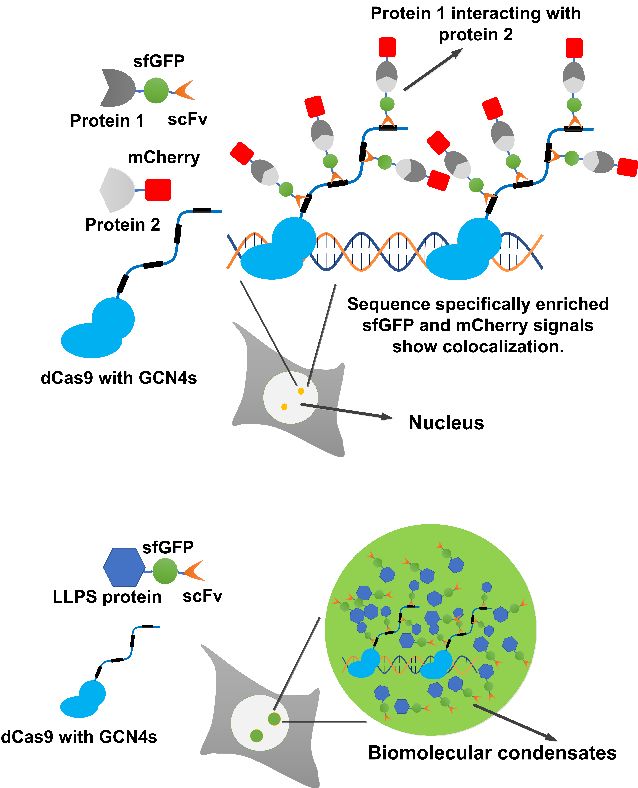
该系统以 CRISPR-dCas9 介导的基因组定位为基础,结合 SunTag 信号放大模块 , 将互作蛋白富集于基因组特定位点,形成高信噪比的共定位荧光信号 。相比传统 FRET 、 BiFC 等手段, MRC 不仅可呈现多蛋白复合体的静态共定位关系,还支持初步的相互作用强度(如亲和力)比较,并具备对动态变化过程的捕捉能力。在相分离研究方面, MRC 进一步拓展了对相分离凝聚体形成机制的研究能力。研究人员不仅可通过该系统快速筛选并验证具有相分离能力的新蛋白或结构域,还可将多蛋白互作整合进相分离研究之中,系统考察蛋白复合物之间的相互作用如何促进凝聚体的形成 , 为解析多蛋白驱动的凝聚体形成机制提供了强有力工具。 该系统 也 可通过空间上的 “ 程序化排布 ” 来操控多个凝聚体的生成,并探索它们之间的互作、融合与排斥行为 。 此外,研究团队将光遗传学九游官网系统引入 MRC 平台,实现在活细胞中通过光控方式将非相分离蛋白招募至可编程凝聚体中,从而增强蛋白聚集与共定位效率。该策略不仅提升了蛋白互作研究的灵敏度,还可调控凝聚体的物理特性,用于调节目标蛋白功能,具备在酶活调控、信号隔离和药物筛选等领域的应用潜力。 另一方面,研究人员还引入量子点探针对凝聚体进行单分子分辨率的成像分析,进一步揭示其内部动态结构与运动行为,为理解多蛋白复合物的亚结构特征提供了更高分辨的技术支撑。 整体而言, MRC 为活细胞中多蛋白复合体的可视化与相分离研究提供了强大技术支持,展现出其在基础研究与合成生物学领域的广阔应用前景。 未来, MRC 系统有望进一步应用于胞质区域乃至细胞器内部的复杂环境中,并与实时动力学建模、药物筛选、人工信号通路构建等策略结合,为基础研究及合成生物学、药物开发等多个方向提供强大技术支撑与新思路。

【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。
特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
女子一手拿电话一手骑电动车摔倒后报警,相隔数米的对向来车被认定负次责因“没有礼让对方优先通过”,车主已申请复议,监控曝光
曝英伟达 RTX 5090 D v2 显卡建议零售价与 5090 D 同为 16499 元
开源E-ink相框Paper 7登场:固件可完全自定义,搭载7英寸彩屏
利民推纵横视界 AIO 同款机箱副屏:6.68 英寸 1280×480,192 元
 热点新闻
热点新闻  联系我们
联系我们 电话:13929967909
座机:0757-83205002
邮箱:19407036@qq.com
地址:广东省佛山市禅城区国际交易中心8座2楼30-31号

